2013年度バイオインダストリー協会 化学・生物素材研究開発奨励賞受賞講演
早稲田大学理工学術院 先進理工学部応用化学科 助教 古屋俊樹先生(新49)
BioJapan2013 World Business Forumにおいて木野研究室の古屋俊樹先生の2013年度バイオインダストリー協会 化学・生物素材研究開発奨励賞の受賞講演が2013年10月9日(水)16:20からパシフィコ横浜展示棟にて行われ、拝聴しましたので報告します。

古屋先生は、『環境調和性の観点からバイオプロセスをより普及させること』をモットーとして、選択性と環境調和性に優れている生体触媒として酸化酵素の有用化合物合成への応用を目的として研究を進めております。
受賞講演のタイトルは、『二核鉄型酸化酵素を利用した高選択酸化プロセスの開発』で、化学プロセスでは困難なフェノールのパラ位選択的酸化反応を二核鉄型酸化酵素により実現し、ヒドロキノンを生産するプロセスを見出しました。従来、メタン酸化細菌や放線菌由来の酸化酵素は、異種細胞内で発現させることが困難で、活性が不十分な自然界から分離した株を実用化するための活性強化も困難でした。
先生は、フェノールのパラ位を選択的に酸化してヒドロキノンに変換するユニークで有用な活性を有し、生体触媒への応用に期待が寄せられているMycobacterium属細菌を利用して当該細菌の遺伝子破壊実験を実施してmimABCD遺伝子群がフェノールのパラ位選択的酸化酵素をコードしていることを解明しました。このMimABCDタンパク質は、二核鉄型酸化ファミリーの酵素であり、4つのコンポーネント、すなわちoxygenase large subunit, reductase, oxygenase small subunitおよびcoupling protein で構成され、それぞれMimA, MimB, MimC, MimDのタンパク質に対応していると推定しました。ついでmimABCD遺伝子をクローニングしてMycobacterium属細菌の近縁のRhodococcus属細菌に導入して変換活性を評価しましたが、フェノール酸化活性は検出されませんでした。
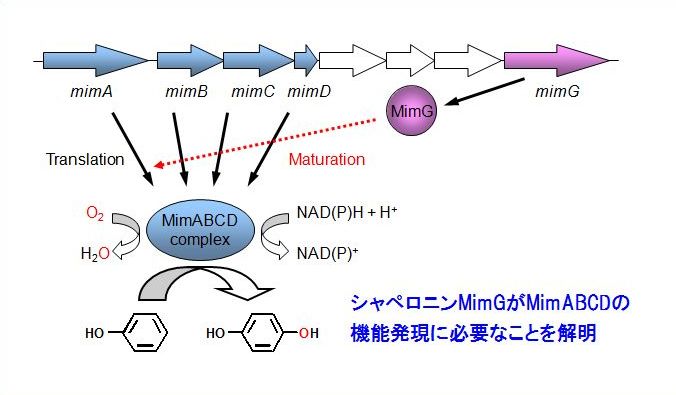
このような状況下、他の要因の存在を予測し、mimABCD遺伝子群の周辺領域のゲノム配列を精査した結果、その下流にGroELファミリーのシャペロニンタンパク質(タンパク質の立体構造形成を補助するタンパク質)と相同性を示すORF Msmeg_1978が存在することを見出しました。文献上ではあまり重要視されていないタンパク質とのことでしたが、この遺伝子(mimGと命名)がMimABCDタンパク質の立体構造形成や活性発現に関与していると予測し、mimABCD遺伝子とmimG遺伝子をRhodococcus細胞内で共発現させた結果、フェノールのパラ位選択的酸化活性を異種細胞内で発現させることに成功しました。さらに、MimGの機能をWestern Blottingにより検討し、MimG非存在下ではMimAタンパク質は不活化し、フェノール酸化活性は検出されませんでしたが、MimGを共存させることによりMimAタンパク質の可溶化が発現し、フェノール酸化活性が検出され、立体構造形成に不可欠であることを見出しました。
以上のように二核鉄型酸化酵素MimABCDタンパク質の活性発現にはシャペロニンタンパク質MimGが不可欠であり、MimGタンパク質機能の解明により異種細胞内で発現させるシステムの基盤を構築することに成功しました。また、MimGタンパク質の発見により当該ファミリー酸化酵素の異種発現や応用に大きなブレークスルーをもたらす可能性を秘めており、現在、ヒドロキノン実生産に向けた高活性株の創製に取り組みつつ、二核鉄型酸化酵素の異種発現や機能開発も発展させていくと力強く締めくくられました。
詳しくは当日の講演抄録をご覧ください ⇒ こちら(pdf資料)
以下に先生から提供された解説図をお示しします。